Nipah Virus
Das Nipah-Virus (NiV) ist ein zoonotisches Paramyxovirus mit wiederkehrenden lokalen Ausbrüchen in Süd- und Südostasien. Aufgrund seiner hohen Letalität (40–75 %) und der fehlenden zugelassenen Impfstoffe oder spezifischer Therapien gehört es zu den von der Weltgesundheitsorganisation (WHO) als High-Priority Pathogen gelisteten Erregern im Rahmen der globalen Forschungsvorbereitung.
Aktuelle Meldungen über bestätigte Fälle in Westbengalen, Indien haben im Januar 2026 wieder Aufmerksamkeit auf NiV gelenkt, was die Bedeutung von Surveillance, Grundlagenforschung und experimentellen Werkzeugen unterstreicht. antibodies-online bietet hochwertige Antikörper und Proteine gegen das Nipah-Virus für Forschung und Testentwicklung an – entdecken Sie unser Sortiment unten.
Nipah Virus Antikörper
Nipah Virus Proteine
Virologie und Pathogenese
NiV gehört zur Familie Paramyxoviridae, Genus Henipavirus. Es besitzt ein einzelsträngiges, negatives RNA-Genom, das für sechs strukturelle Proteine kodiert: N (Nukleokapsid), P (Phosphoprotein), M (Matrix-Protein), F (Fusionsprotein), G (Attachment-Glykoprotein) und L (RNA-abhängige RNA-Polymerase).
Das G-Protein vermittelt die Bindung an zelluläre Rezeptoren (Ephrin-B2 und Ephrin-B3), während das F-Protein die Fusion der viralen Hülle mit der Zellmembran katalysiert – zentrale Schritte beim Eintritt in die Wirtszelle.
Die Übertragung auf den Menschen erfolgt typischerweise durch Kontakt mit kontaminierten Nahrungsmitteln (z. B. durch Fruchtfledermausspeichel kontaminierte Palmensäfte) oder direkte Exposition zu infizierten Tieren oder Personen. Mensch-zu-Mensch-Übertragung ist dokumentiert, besonders in Gesundheits- und Pflegeeinrichtungen.
Epidemiologische Situation: Aktuelle Ausbrüche und Historie
Im Januar 2026 bestätigten indische Behörden zwei Fälle von NiV-Infektionen im Bundesstaat Westbengalen, beide bei medizinischem Personal. Insgesamt wurden 196 Kontaktpersonen identifiziert, alle bisher asymptomatisch und negativ getestet. Behörden erklärten den Ausbruch als eingegrenzt, doch mehrere Länder in Süd- und Südostasien verstärken Grenzkontrollen und Gesundheitsüberprüfungen.
Ältere Ausbruchsmuster zeigen, dass NiV in Indien wiederholt lokal auftritt. In den letzten Jahren wurde NiV in Kerala fast jährlich registriert, mit unterschiedlich hohen Fallzahlen und Fallsterblichkeiten, was die anhaltende Präsenz und das Krankheitsrisiko in endemischen Gebieten illustriert.
Das Virus wurde erstmals in den Jahren 1998–1999 bei Ausbrüchen in Malaysia und Singapur identifiziert. Später traten wiederholt Fälle in Bangladesch und Indien auf, oft durch Spillover von Fruchtfledermäusen.
Klinische Manifestation und Risiko
Die Inkubationszeit beträgt typischerweise wenige Tage bis mehrere Wochen. Die klinischen Symptome reichen von unspezifischen grippeähnlichen Beschwerden bis zu schweren respiratorischen Erkrankungen und hämorrhagischer Enzephalitis, die letal verlaufen kann.
Da keine spezifisch zugelassenen Behandlungen oder Impfstoffe existieren, beschränkt sich die Therapie auf supportive Maßnahmen und Infektionskontrolle.
Forschungsbedarf und Herausforderungen
Trotz über 25 Jahren Kenntnis des Erregers bestehen bedeutende wissenschaftliche Lücken, vor allem bei den Wirt-Pathogen-Interaktionen, der Immunantwort und der therapeutischen Entwicklung. Forschung in diesen Bereichen ist wegen der Bio-Sicherheitsanforderungen (BSL-4) komplex und aufwändig.
Eine internationale Konsolidierung von Assays, Modellen und Standardreagenzien ist für zuverlässige Ergebnisse und Vergleichbarkeit zwischen Laboren notwendig, wie aktuelle Forschungsübersichten betonen.
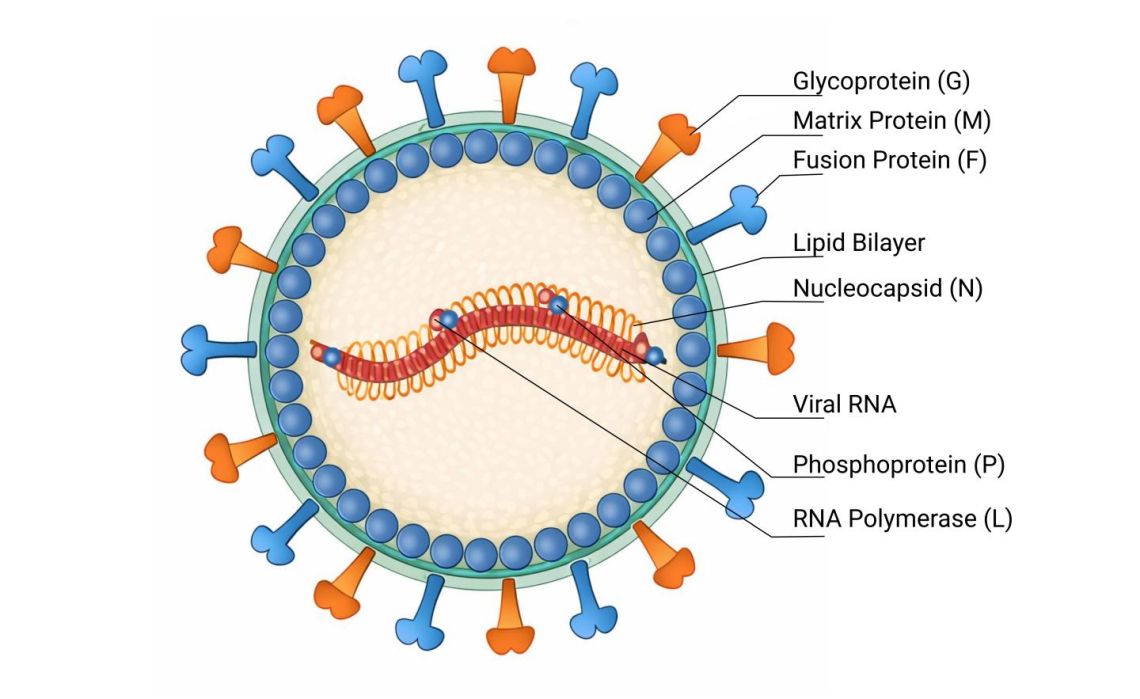
Fig. 1: Schematische, farbcodierte Querschnittsdarstellung des Nipah-Virus mit beschrifteten Strukturkomponenten, einschließlich Lipidmembran, Glycoprotein (G), Fusionsprotein (F), Matrixprotein (M), Nukleokapsid (N), viraler RNA sowie Phosphoprotein (P) und RNA-Polymerase (L).
Experimentelle Werkzeuge: Antikörper und Assays
Für nicht-infektiöse experimentelle Kontexte sind zielgerichtete Antikörper gegen virale Proteine zentrale Werkzeuge:
Antikörper gegen G-Protein (Attachment) zur Analyse der Rezeptorbindung und zur Charakterisierung von Oberflächenstrukturen bei pseudotypischen Systemen.
Antikörper gegen F-Protein (Fusion) zur Untersuchung der Membranfusionsmechanismen und in Screening-Assays für Eintrittsinhibitoren.
Antikörper gegen N-Protein dienen primär der quantitativen Erfassung von Virusprotein-Expression in transgenen Systemen oder in virologischen Modellierungen.
Solche Reagenzien sind ausschließlich für Forschungszwecke (RUO) validiert und ermöglichen kritische Einblicke in Viruseigenschaften ohne Arbeit mit infektiösem Material.
Zur Unterstützung der experimentellen Nipah-Virus-Forschung sind bei antibodies-online.com polyklonale und monoklonale Antikörper gegen relevante virale Strukturproteine verfügbar, die in protein- und zellbasierten Assays eingesetzt werden können.
Nipah Antikörper und Proteine anschauen
Schlussfolgerung
Das Nipah-Virus bleibt ein wichtiges Zielgebiet für globale Forschung, nicht wegen einer hohen globalen Fallzahl, sondern aufgrund seines hohen Krankheitsgewichts, wiederkehrender lokaler Ausbrüche und seiner Pandemie-Relevanz. Fortschritte in Diagnostik, immunologischer Charakterisierung und präklinischen Modellen sind essenziell. Standardisierte, gut charakterisierte experimentelle Werkzeuge — etwa spezifische Antikörper gegen virale Strukturproteine — tragen maßgeblich dazu bei, diese Herausforderungen zu adressieren.
Referenzen:
- National Centre for Disease Control (India) – Nipah Virus Disease Alert, Januar 2026
- UK Health Security Agency – Nipah virus: what is it, where is it found and how does it spread? (2026)
- Hantabal et al. – Current knowledge on host–pathogen interactions of henipaviruses (ScienceDirect, 2026)
- Madhukalya R. – Nipah virus: pathogenesis, genome, diagnosis, and treatment (PubMed, 2025)
- Zhou D. et al. – Antigenic landscape of Nipah virus attachment glycoprotein (Nature, 2025)
- Reuters – India reports two Nipah virus infections as regional screening is stepped up (Jan 2026)
- Associated Press – India says Nipah virus outbreak contained (2026)




